云南省第一人民医院药物临床试验机构工作公示信息
一、国家药物临床试验机构基本信息
职务 | 姓名 |
主任 | 蒋立虹 |
副主任 | 梅妍 |
办公室主任 | 曹玮 |
机构秘书 | 罗铁成 |
质控员 | 刘佳 |
药品管理员 | 曹俊东 |
机构邮箱 | khjg_yn@163.com |
机构电话 | 0871-63662173 |
机构传真 | 0871-63662167 |
接待时间段 | 每周一周二:上午:8:00-12:00 下午:14:00-18:00 |
办公室地址 | 云南昆明市金碧路157号云南省第一人民医院2号门诊楼13楼机构办公室 |
NMPA备案专业 | 肿瘤、血液、消化、神经内科、内分泌、呼吸、传染、肾病、临床心理、麻醉、眼科、心血管、免疫、生殖健康与不孕不育(生殖妇科) |
备案编号 | 药临床机构备字2020000161 |
邮编 | 650032 |
开展项目 | Ⅱ期药物临床试验(√) |
机构官方网站 | http://www.ypfph.com |
1、机构概况
云南省第一人民医院药物临床试验机构于2013年12月通过CFDA的资格认定,2020年进行备案。机构设立了机构办公室,负责全院药物临床试验的组织、实施、协调和监督等日常工作。机构现有14个专业具有药物临床试验资格,包括肿瘤、消化、内分泌、血液、神经内科、呼吸、免疫、传染、心血管、临床心理、肾病、生殖妇科、眼科、麻醉。机构配备了专职的机构秘书、质控员及药品管理员,有效保证所承接项目顺利完成。
备案PI具体可以在国家药品监督管理局查询,查询网址https://beian.cfdi.org.cn/CTMDS/apps/pub/drugPublic.jsp#
药物临床试验机构组织架构图
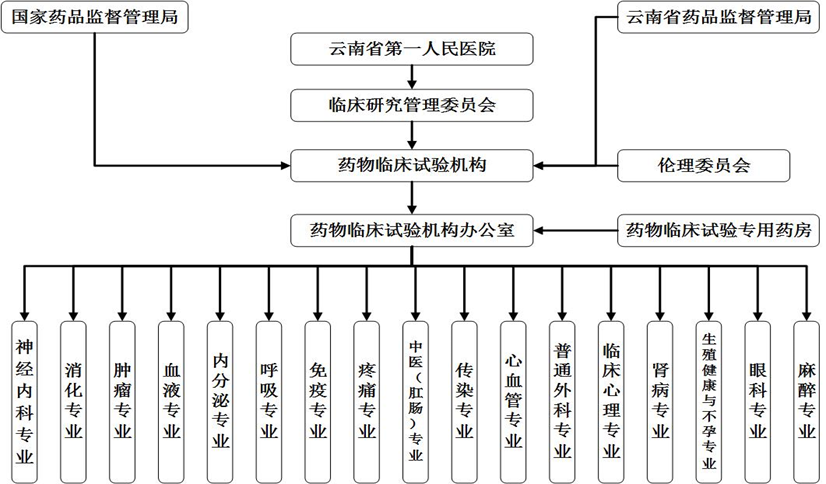
2、机构办事流程

3、药物临床试验立项申请资料目录
试验名称:
申办方: 提交日期:
序号 | 材料名称 | 版本号及日期 |
1. | 报送资料目录 | |
2. | 立项申请表(申办者及研究者) | |
3 | 国家食品药品监督管理总局批件 | |
4. | 药物临床试验委托书 | |
5. | 申办者/CRO对项目经理、监查员的授权委托书 | |
6 | 申办者对CRO的委托函(如适用) | |
7 | 监查员/CRC相关资质文件(个人简历及GCP培训证书、派遣函、身份证复印件) | |
8 | 组长单位伦理批件 | |
9 | 申办者/CRO资质证明(药品生产许可证、GMP证书、营业执照复印件,注明原件复印,单位原章), 拟合作的SMO公司资质证明 | |
10 | 试验方案及其修正案(方案上应有本院课题负责人、申办方临床试验负责人签名) | |
11 | 病例报告样表 | |
12 | 研究者手册 | |
13 | 知情同意书样本、其他提供给受试者的任何书面资料、招募广告(若有) | |
14 | 试验药物的标签及药检证明 | |
15 | 药品注册批件及进口药品注册证(上市后药品) | |
16 | 试验药物的药品说明书(上市后药品) | |
17 | 主要研究者简历及医师资格证、职称证书、注册证、GCP培训证书复印件 | |
18 | 药物临床试验研究团队成员表、简历、GCP证书 | |
19 | 方案涉及的公司不涉外承诺书(如适用) | |
20 | 在试验方案中涉及的医学、实验室、专业技术操作和相关检测的参考值和参考值范围 | |
21 | 医学、实验室、专业技术操作和相关检测的资质证明(资质认可证书或者资质认证证书或者已建立质量控制体系或者外部质量评价体系 或者其他验证体系) | |
22 | 盲法试验的揭盲程序 | |
23 | 试验启动监查报告 | |
24 | 方案研讨会(研究者会会议记录) | |
25 | 其他材料(如受试者日记卡和其他问卷表、用、保险证明等) |
备注:请以上材料请按照清单顺序装订,3-16及19-25项需加盖提供单位红章。
签收:
4、合同签署流程
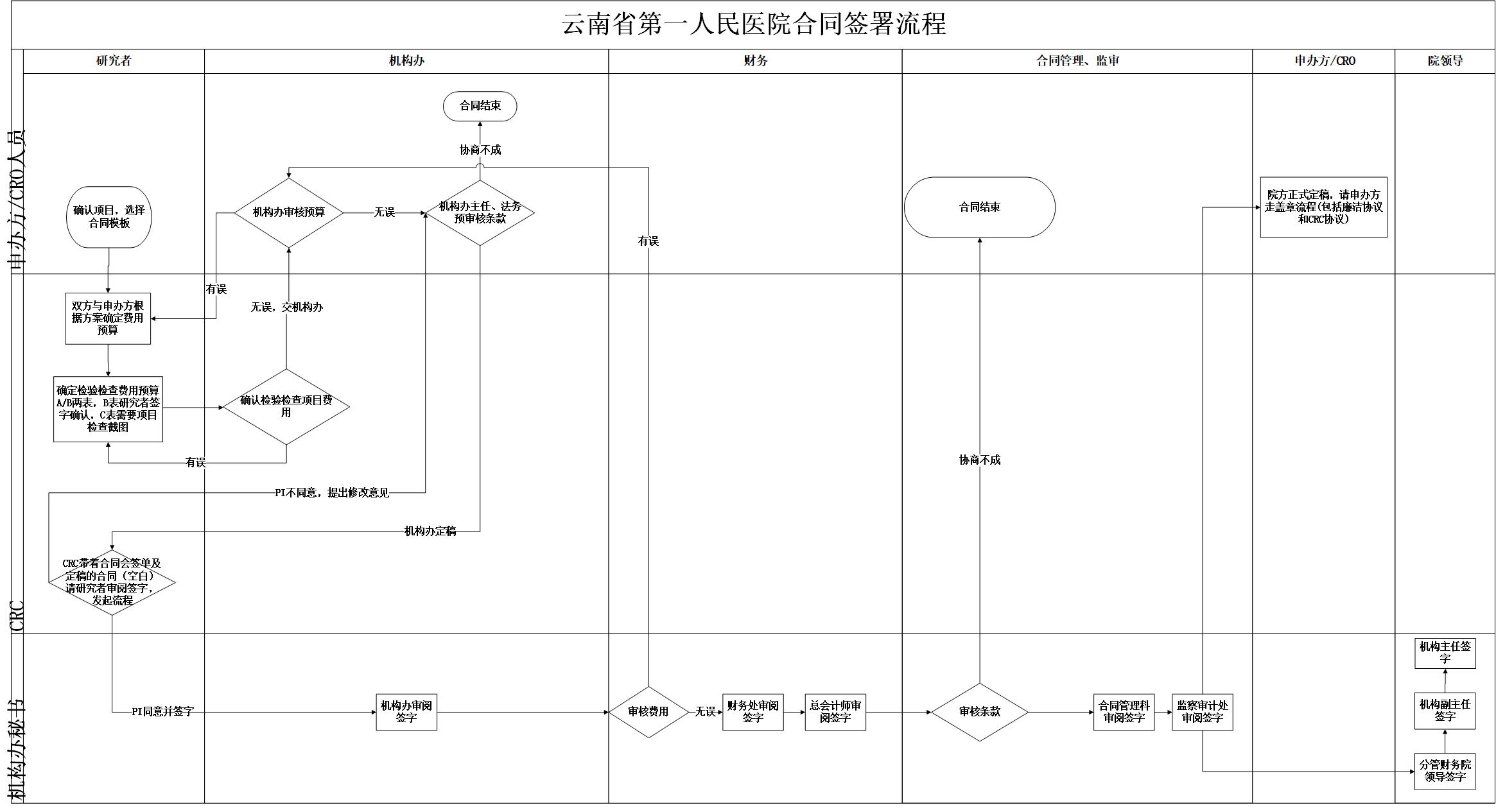
5、关中心流程
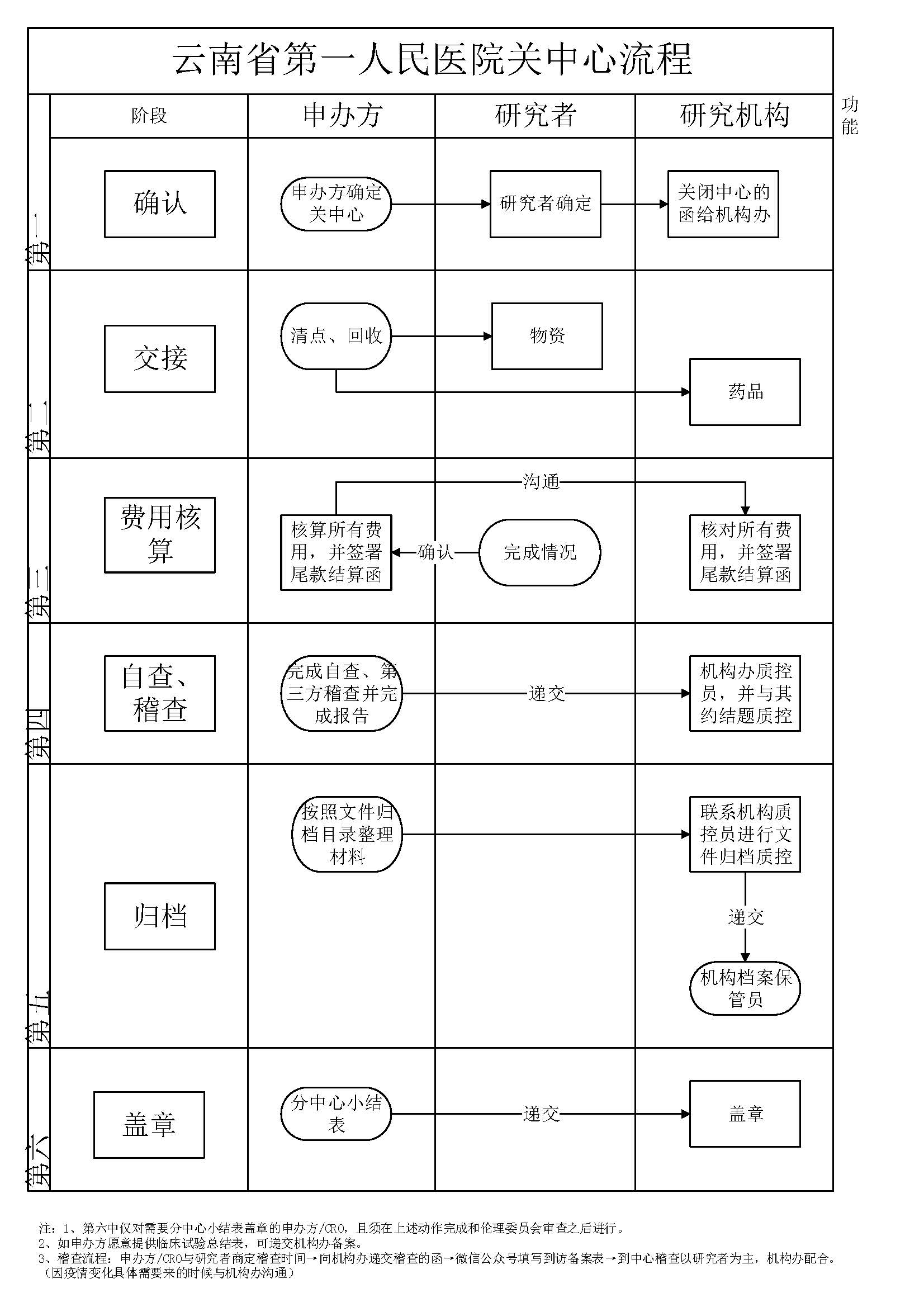
发布时间:2023-04-10

